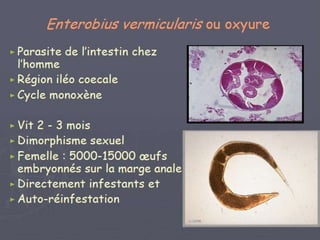
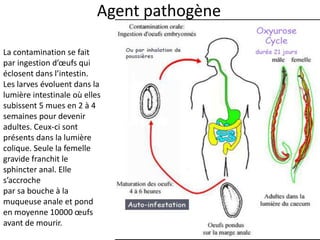
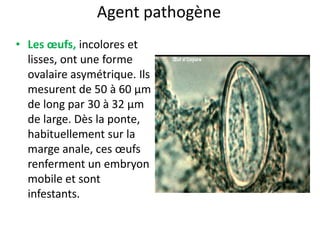
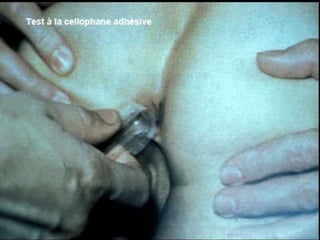
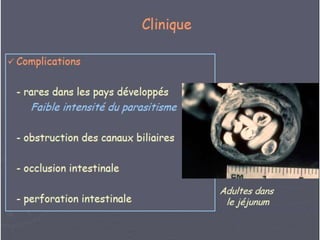
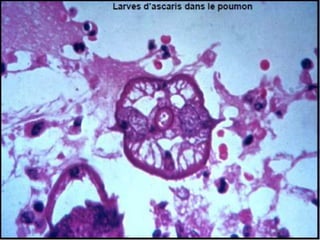
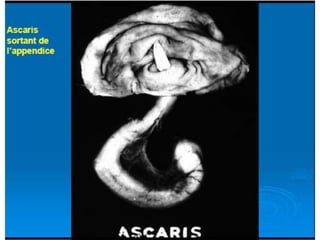
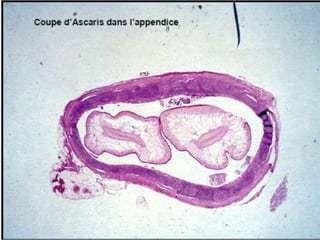
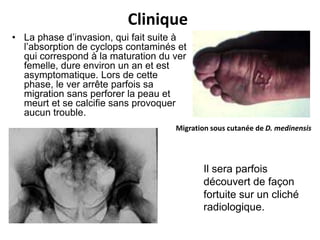
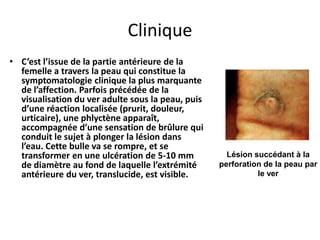
Le document présente des généralités sur les nématodes, notamment leur classification en fonction de leur mode de transmission et décrit plusieurs parasitoses intestinale causées par des nématodes, telles que l'oxyurose, l'ascaridiose, la trichocéphalose, la trichinellose et la dracunculose. Chaque parasitose est accompagnée d'informations sur l'agent pathogène, le cycle de vie, la clinique, le diagnostic et le traitement. La dracunculose, par exemple, est une affection tropicale en déclin grâce aux efforts d'éradication, tandis que la trichinellose est généralement contractée par la consommation de viande contaminée.