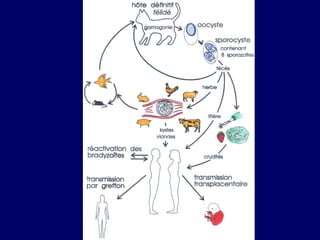
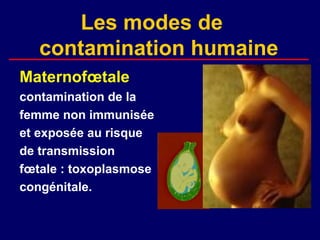
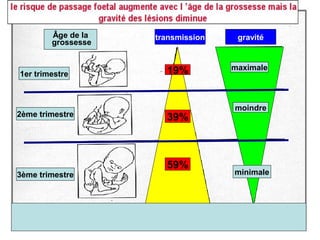
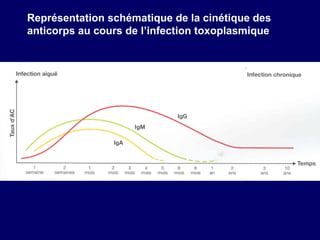
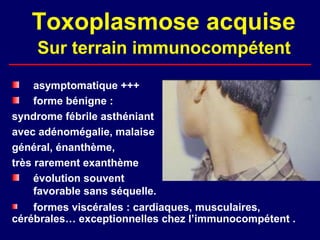
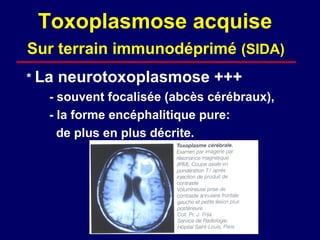
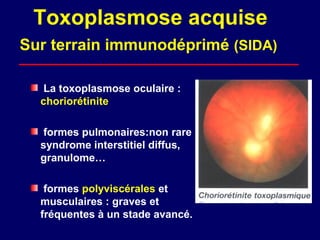
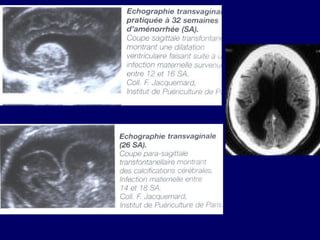
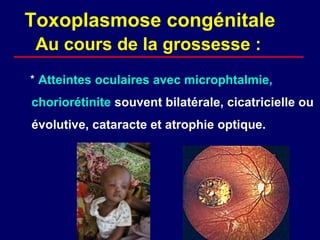
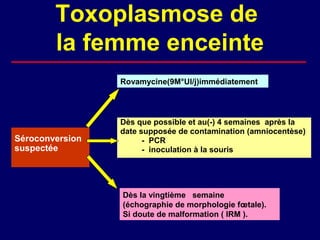
La toxoplasmose est une zoonose causée par Toxoplasma gondii, touchant principalement les mammifères et les oiseaux, avec des formes cliniques acquises et congénitales. Le cycle évolutif du parasite comprend des phases asexuées et sexuées, et la contamination humaine se produit principalement par ingestion d'oocystes ou de kystes présents dans la viande crue. Le diagnostic et le traitement varient en fonction des formes cliniques et de l'état immunitaire du patient, nécessitant une attention particulière pour les femmes enceintes et les individus immunodéprimés.