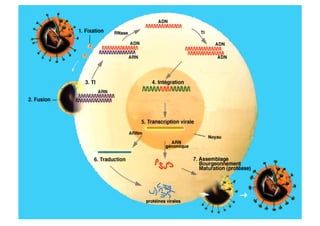
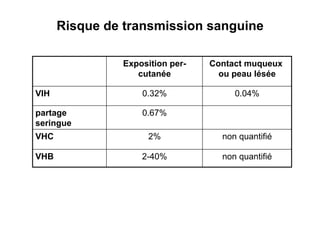
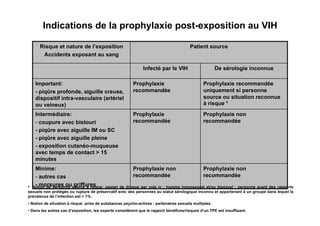
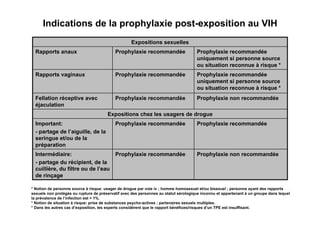
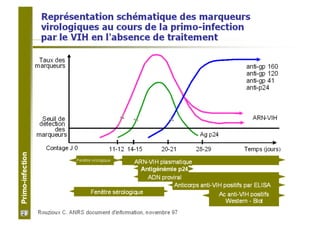
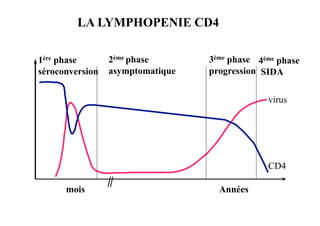
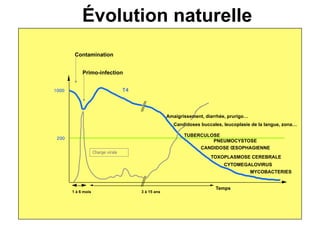
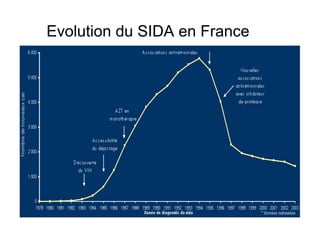
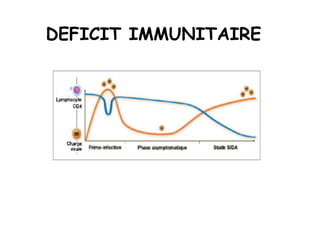
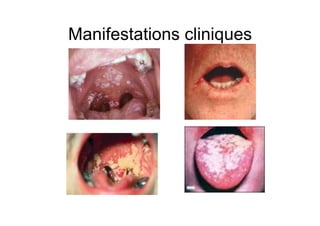
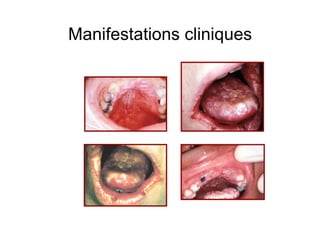
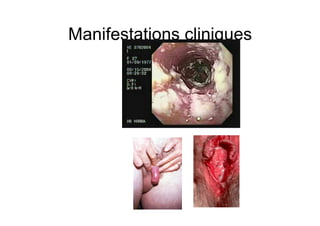
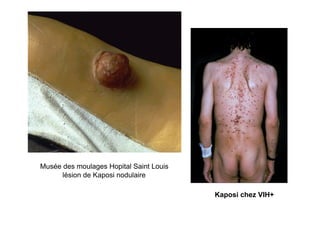
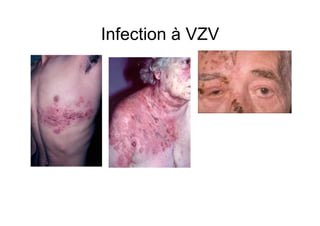
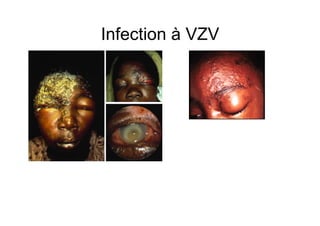
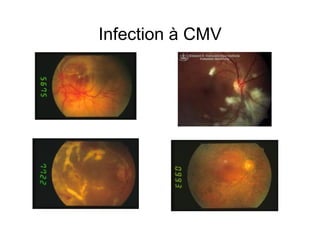
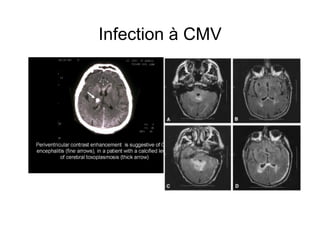
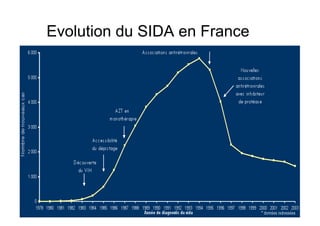
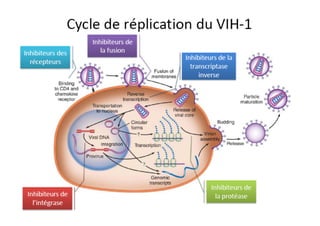
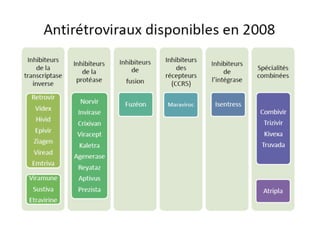
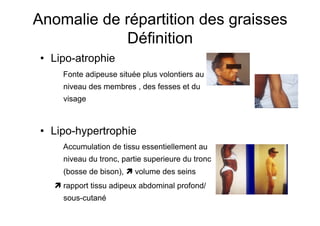
Le document explore l'histoire naturelle de l'infection par le VIH, soulignant les origines du virus, les phases de l'infection et les mécanismes de transmission. Il traite des risques associés à la transmission sanguine, sexuelle et materno-fœtale, ainsi que des stratégies de prévention et des recommandations en cas d'exposition. Des aspects biologiques, comme le taux de CD4 et la charge virale, sont également abordés pour comprendre l'évolution de la maladie et l'importance du dépistage.