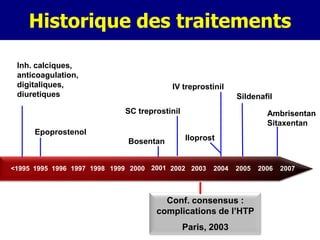
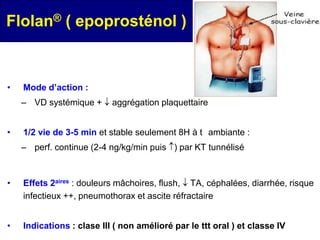
L'hypertension porto-pulmonaire (HTPP) est une complication associée à diverses pathologies hépatiques et pulmonaires, avec des causes et groupements variés. Elle se caractérise par une pression artérielle pulmonaire moyenne (PAPM) supérieure à 25 mmHg et peut nécessiter des traitements spécifiques incluant des anticoagulants, des inhibiteurs calciques et des thérapies ciblées, notamment pour améliorer le pronostic des patients. Le diagnostic repose sur des critères cliniques et hémodynamiques, et la gestion des cas peut inclure la transplantation hépatique en fonction de la sévérité de l'hypertension.




















![Critères diagnostiques
1. HTP +/- cirrhose ( thrombose porte, HNR, FHC, Budd-Chiari )
2. Hypoxémie artérielle : gradient artério-alvéolaire > 15
mmHg ( > 20 mmHg chez patients > 64 ans )
AaDO2 (mmHg) = [0,21 x (PB – 47)] - (PaCO2 / 0,8) - PaO2
= 150 - (PaCO2 / 0,8) - PaO2
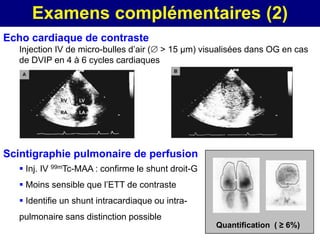
3. Dilatations vasculaires intra-pulmonaires démontrées par :
- Echocardiographie de contraste, ou
- Scintigraphie de perfusion (99mTc MAA )
Rodriguez-Roisin et al. Eur Resp J 2004;24:861-80](https://image.slidesharecdn.com/htpp-des-thevenot-120612131039-phpapp01/85/Htpp-des-t-hevenot-27-320.jpg)