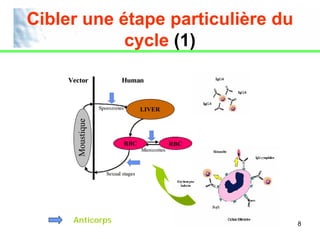
Le document aborde la sélection des antigènes pour les essais cliniques de vaccins contre le paludisme, en discutant des critères de choix tels que la non-toxicité et l'immunogénicité. Il souligne les stratégies pour accélérer l'acquisition de l'immunité naturelle et cibler des étapes spécifiques du cycle parasitaire. Enfin, il détaille les phases des essais cliniques, de la phase I à IV, en décrivant leurs objectifs respectifs.